近日,远大医药(0512.HK)核药领域战略合作伙伴澳洲Telix公司(ASX: TLX; NASDAQ: TLX)传来重磅利好,其用于治疗前列腺癌的全球首创(first-in-class)的镥标记的治疗性放射性抗体药物偶联物(rADC)候选药物TLX591-Tx国际多中心III期临床试验(ProstACT Global)的第一部分(安全性和剂量学引导)已成功达到主要目标,证明了该产品的安全性和耐受性,且未观察到新的不良反应,不仅促进了该创新产品未来的进一步开发及上市,同时也体现了前列腺癌治疗未来有望获得全新选择。
全球首创疗法优势破局,差异化靶向提供全新治疗选择
据悉,TLX591-Tx为全球首创镥标记的治疗性rADC,其靶向性和药理学特性与现有已上市的前列腺特异性膜抗原(PSMA)靶向小肽分子显著不同,旨在实现高内化率、长滞留时间和对PSMA的高度选择性。
本次获得进展的ProstACT Global是一项随机、开放标签的国际多中心III期临床试验,旨在评估TLX591-Tx联合标准疗法(阿比特龙、恩扎卢胺或多西他赛)对比单独使用标准疗法治疗PSMA阳性的转移性去势抵抗性前列腺癌 (mCRPC)患者。
ProstACT Global试验分为两部分:第一部分为安全性和剂量学导入期,已完成全部36例患者的入组;第二部分为2:1随机分组的全球扩展研究,拟入组约490例患者。该试验入组的患者必须经68Ga-PSMA-11 PET显像剂确诊为mCRPC,如远大医药全球创新放射性核素偶联药物(RDC) TLX591-CDx (Illuccix®);此外,患者还需接受过一种雄激素受体通路抑制剂(ARPI)治疗。未来,该III期临床试验第一部分的数据将会递交予美国食品药品监督管理局(FDA),以推进在美国开展第二部分的研究。同时,该试验第二部分的患者招募将在已获批开展临床的地区(包括中国大陆)同步推进。
本次ProstACT Global试验第一部分主要研究结果证实了TLX591-Tx的安全性及耐受性良好,试验血液学事件均为短暂且可控,同时剂量学数据也证实了肿瘤摄取。此外,与其他PSMA靶向小分子放射性配体疗法(RLT)相比,TLX591-Tx治疗展现了出不同的靶向性和药理学特性。根据对TLX591-Tx治疗患者的长期随访,未观察到明显的急性或迟发性肾毒性;同时,由于其分子量较大,TLX591-Tx在唾液腺和泪腺的摄取也极低,从而减少了口干和眼干的副作用。
创新产品矩阵剑指百亿蓝海市场,“Go Global”战略夯实核药领军地位
前列腺癌是我国男性群体中常见的癌症类型之一,且其发病率和病死率正随着人口老龄化加剧等因素呈明显升高趋势。根据弗若斯特沙利文数据,预计2025年我国前列腺癌患者数约为108万人,预计前列腺癌药物市场规模将于2030年增长至近506亿元人民币,而同期全球市场规模则将达约376亿美元。
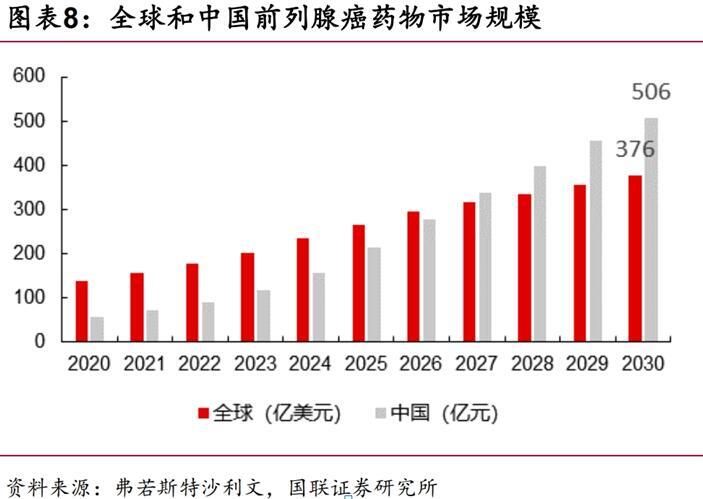
针对这一市场潜力巨大的蓝海市场,远大医药已前瞻性地布局了多款创新产品,包括前列腺癌诊疗全球创新RDC产品组合TLX591-CDx及TLX591,以及用于前列腺癌早检的创新产品优护。
以TLX591-CDx为例,该产品的靶向剂PSMA-11能以高亲和力的方式特异性结合在前列腺癌中高表达的PSMA上,具有可内化入细胞、生物学活性稳定、体内循环半衰期短以及对肿瘤实质的渗透性好且可被非靶向组织快速清除的五大特点。TLX591-CDx在海外上市后销售数据保持高速增长,2025年全年取得了超过6亿美元的收入,同比增长超20%。目前该产品已在国内的新药上市申请(NDA)已获受理,未来将为我国前列腺癌患者带来全球领先的精准诊断工具,为疾病的早期发现、精准分型与治疗方案优化提供全新可能。
前列腺癌诊疗领域的优势布局,是远大医药多年来在核药抗肿瘤诊疗领域持续深耕的必然结果。作为全球核药抗肿瘤诊疗领域的领军企业之一,远大医药已在核药板块实现了研发、生产、配送、销售等多个环节的全方位布局。公司以波士顿、成都为核心的研发基地,波士顿、法兰克福、新加坡、成都所在的生产基地以及覆盖全球50多个国家和地区的销售网络为基础,实现了核药产业链全球化布局。
产品方面,围绕肿瘤诊疗一体化的治疗理念,公司在研发注册阶段已储备16款创新产品,涵盖68Ga、177Lu、131I、90Y、89Zr在内的5种放射性核素,覆盖了肝癌、前列腺癌、脑癌等在内的7个癌种;在早期研发阶段,以RDC药物为主,产品储备达10余款,产品种类涵盖诊断和治疗两类核素药物,为患者提供多适应症治疗选择、多手段且诊疗一体化的全球领先的抗肿瘤方案。
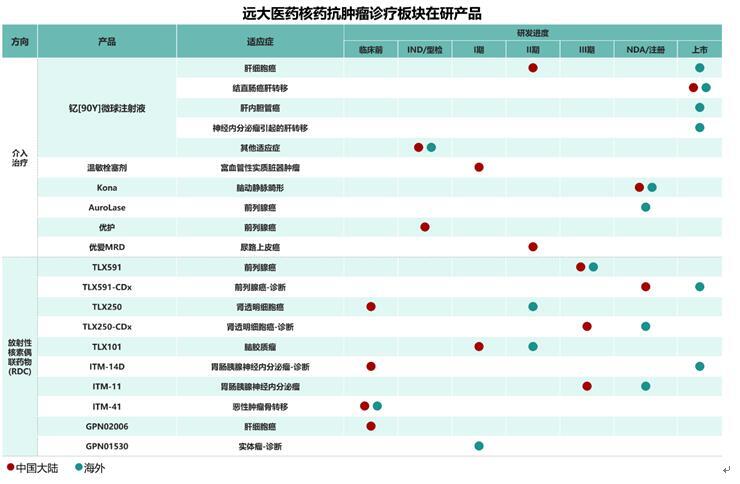
值得注意的是,公司自主研发的全球创新靶向成纤维细胞活化蛋白(FAP)的小分子RDC药物GPN01530早前已获得FDA批准开展用于诊断实体瘤的I/II期临床研究,成为远大医药首款获得FDA批准开展临床研究的自研RDC产品,该产品在临床前研究中已展现出“同类最优”(BIC)潜质,或将成为下一代癌症成像标准疗法。该产品海外临床的成功获批也为远大医药核药产品管线的国际化开发提供了重要范式,同时也展现出了公司核药技术平台优秀的临床前开发及国际注册能力。同时,公司全球创新、基于放射性核素-抗体偶联技术的靶向磷脂酰肌醇蛋白聚糖3 (GPC-3)的诊断型放射性药物GPN02006早前在中国开展的研究者发起的临床研究(IIT临床研究)取得了里程碑式突破,并在2025年北美核医学与分子影像学会(SNMMI)年会斩获口头报告,该产品极具潜力,有望成为全球首个针对GPC-3靶点的肝细胞癌(HCC)诊断类RDC产品。
产业链方面,远大医药位于四川成都的放射性药物研发及生产基地已正式投入运营,其配备了14条高标准GMP生产线,且实现了100%自主生产,彻底破解了核药领域的“卡脖子”难题,摆脱了进口依赖。该基地是全球首个核药全产业链闭环平台,也是目前国际范围内核素种类最全、自动化程度最高的智能工厂之一,可充分满足公司治疗性与诊断性核药的多品种、规模化制备需求。
未来,随着全球核药市场的持续扩容,远大医药有望凭借其先发优势与全产业链能力,深入践行其“Go Global”的发展战略,进一步扩大公司在全球核药市场的份额,为全球肿瘤患者提供更优质的诊疗方案,同时推动中国核药产业在全球舞台上实现进一步突破。
(责任编辑:杨秀峰)